题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于下列反应,(298.15K)=172.5 kJ·mol-1,若增大总压力或升高温度或加人催化剂,则反应速率常数k正、k逆,和反
对于下列反应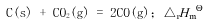 (298.15K)=172.5 kJ·mol-1,若增大总压力或升高温度或加人催化剂,则反应速率常数k正、k逆,和反应速率υ正、υ逆,以及标准平衡常数
(298.15K)=172.5 kJ·mol-1,若增大总压力或升高温度或加人催化剂,则反应速率常数k正、k逆,和反应速率υ正、υ逆,以及标准平衡常数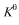 、平衡移动方向等将如何?分别填入表2-1中。
、平衡移动方向等将如何?分别填入表2-1中。
表2-1 | ||||||
k正 | k逆 | v正 | v逆 | K^{ominus } | 平衡移动方向 | |
增加总压力 | ||||||
升高温度 | ||||||
加入催化剂 |
 答案
答案





 ,已知某温度下正反应速率常数k正=1,逆反应速率常数k逆=0.5,则处于平衡状态的体系是
,已知某温度下正反应速率常数k正=1,逆反应速率常数k逆=0.5,则处于平衡状态的体系是 Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。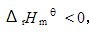 ,当达到平衡后,再适当降低温度则正反应速率将______,逆反应速率将______,平衡将向______方向移动;平衡常数将______。
,当达到平衡后,再适当降低温度则正反应速率将______,逆反应速率将______,平衡将向______方向移动;平衡常数将______。