 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。”相关的问题
更多“已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。”相关的问题
第1题
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离平衡常数Ksp约为______;将该溶液稀释后,其pH将变______,解离度α将变______,其将______。
第2题
第4题
某一元弱酸HA的浓度为0.010mol·L-1,在常温下测得其pH为4.0。求该一元弱酸的解离平衡常数和解离度。
第5题
已知某一元弱酸的钠盐NaX0.20mol·L-1溶液pH=9.0,试计算该弱酸HX的解离常数Ka。
第6题
取0.10mol·L-1的某一元弱酸(HA)50.0mL与20.0mL、0.10mol·L-1KOH溶液混合,将混合溶液稀释至100mL,测得此溶液的pH值为5.25,问此一元弱酸的Ka值是多少?
第9题
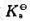 。
。