 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
化学反应速率式为A力K表示的速率常数为P,则rKCCCAB为K,如用浓度表示的速率常数KCKC,用压P=__()
A.KCKC
B.KKCC
C.KCCK
D.KCCK
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.KCKC
B.KKCC
C.KCCK
D.KCCK
 答案
答案
 更多“化学反应速率式为A力K表示的速率常数为P,则rKCCCAB为K,如用浓度表示的速率常数KCKC,用压P=__()”相关的问题
更多“化学反应速率式为A力K表示的速率常数为P,则rKCCCAB为K,如用浓度表示的速率常数KCKC,用压P=__()”相关的问题
第2题
反应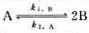 ,式中k1.B为用B表示的正反应速率常数,k2.A为用A表示的逆反应速率常数,平衡常数Kc等于,().
,式中k1.B为用B表示的正反应速率常数,k2.A为用A表示的逆反应速率常数,平衡常数Kc等于,().
A.k1.B/k2.A
B.k1.B/(2k2.A)
C.2k1.B/k2.A
D.2k1.A/k1.B
第3题
以纯A为原料在连续釜式反应器中生产P,反应式为
A→P rP=k1cA
A→U rU=k2cA
式中,反应速率常数k1,k2与温度的关系符合阿伦尼乌斯方程,指前因子A1=4.368×105h-1,A2=3.533×1018h-1,反应活化能E1=41800J/(mol·K),E2=141000J/(mol·K)。若空时为1h,试问在什么温度下操作P的收率最大?
第4题
微生物反应一般在常温附近进行时,其反应速率常数k与温度的关系可以用下式表示:
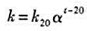
式中: k20为20℃时的反应速率常数; α为温度变化系数;t为温度,℃。
试给出α与Arrhenius公式中活化能Ea的关系式。
第5题
反应N2O5+NO→3NO2在25℃时进行.第一次实验:
pi(N2O5)=1.0X102Pa,pi(NO)=1.0X104Pa(pi表示初始分压力),以Inp(N2O5)对t作图得一直线,由图还求得N2O5的半;衰期为2h;第二次实验:pi(N2O5)=pi(NO)=5.0X103Pa,并测得下列数据:
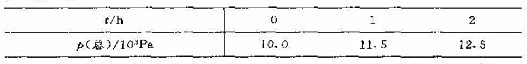
(1)设实验的速率公式形式为r=k[p(N2O5)]α[p(NO)]β.试求α、β值,并求算反应的表观速率常数k值;
(2)设该反应的机理为:
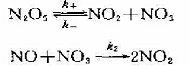
试推断在怎祥的条件下,由该机理导出的速率公式能够与实验结果一致?
(3)当pi(N2O5)=1.00X104Pa,pi(NO)=1.0X102Pa,NO反应掉一半器要多少时间?
第6题
A.活化能的大小不一定能表示一个反应的快慢,但可以表示一个反应受温度的影响是显著还是不显著
B.任意两个反应相比,速率常数k较大的反应,其反应速率必然大
C.任意一个反应的半衰期(t1/2)都与反应的浓度无关
D.任意一种化学反应的速率都与反应物浓度的乘积成正比
第7题
设有一n级反应(n≠1)。若反应物的起始浓度均为a,证明其半衰期公式(式中k为速率常数)为
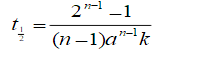
第8题
液相反应A+B→P,反应动力学方程式(-rA)=kcAcB,25℃时反应速率常数k=9.92×10-6m3/(mol·s),物料初始浓度cA0=0.1kmol/m3,cB0=0.08kmol/m3,求在PFR中反应器出口限制反应物转化率为0.95时所需的空时。
第9题
微生物反应一般在常温附近进行时,其反应速率常数k与温度的关系可以用下式表示:
k=k20αt-20
式中:k20——20℃时的反应速率常数;
α——温度变化系数;
t——温度,℃。
试给出α与Arrhenius公式中活化能Ea的关系式。
第10题
乙烯直接水合制乙醇的反应速率式为(-rA)=kcA,在300℃,7MPa,有效扩散系数De=7.04×10-4cm2/s,反应速率常数k=0.09s-1,采用球形颗粒5mm催化剂,试问颗粒内扩散影响程度。
第11题
在间歇釜式反应器中进行液相反应A+B→P,测得二级反应速率常数:k=61.5×10-2L/(mol·h),cA0=0.307mol/L,计算当cB0/cA0=1和5时,转化率分别为0.5,0.9,0.99时所需反应时间,并对计算结果进行讨论。