 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
常压下,水煤气(H2.CO)中CO完全燃烧时可以放出大量的热,这说明此反应:()。
A.ΔH<0
B.ΔS<0
C.不能自发进行
D.ΔS>0
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.ΔH<0
B.ΔS<0
C.不能自发进行
D.ΔS>0
 答案
答案
 更多“常压下,水煤气(H2.CO)中CO完全燃烧时可以放出大量的热,这说明此反应:()。”相关的问题
更多“常压下,水煤气(H2.CO)中CO完全燃烧时可以放出大量的热,这说明此反应:()。”相关的问题
第1题
已知水煤气反应为C(s)+H2O(g)→CO(g)+H2(g),求标准状态时该反应自发进行的最低温度。
第2题
常温常压下B2H6(g)燃烧放出大量的热
B2H6(g)+3O2(g)====B2O3(s)+3H2O(l)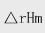 =-2167.2kJ·mol-1
=-2167.2kJ·mol-1
相同条件下Imol单质硼燃烧生成B203(s)时放热636.7kJ,H2O(l)的标准摩尔生成焓为-285.8kJ·mol-1,求B2H6(g)的标准摩尔生成焓。
第3题
 CO2+H2)
CO2+H2)
第4题
将水蒸气通过灼热的煤制备水煤气时的主要反应为:C(s)+ H2O(g)=CO(g)+H2(g),副反应为:C(s)+2H2O(g)=CO2(g)+2H2(g)。将此混合气体冷却至室温即为水煤气,其中含CO、H2和少量CO2,水蒸气可以忽略不计。试计算25℃、100kPa时燃烧1dm3水煤气放出的热量,假设产物均为气体。(1)若只计主反应;(2)若有95%的C(s)生成CO,5%的c(s)生成C02。已知:△fHmθ(H2O,g)=-241.82kJ.mol-1,△fHmθ(CO2,g)=-393.51kJ.mol-1,△fHmθ(CO,g)=-110.53kJ.mol-1。
第7题
298K时,在恒容量热计中测得1.00molC6H6(1)完全燃烧生成H2O(1)和CO2(g)时,放热3263.9kJ。计算恒压下1.00molC6H6(1)完全燃烧时的反应热效应。
第8题
B2H6按下式进行燃烧反应:
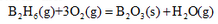 25℃常压下,每燃烧1molB2H6(g)放热2020kJ,同样条件下2mol元素硼燃烧生成1molB2O3(S),放热1264kJ。求25℃时B2O6(g)的标准摩尔生成焓。
25℃常压下,每燃烧1molB2H6(g)放热2020kJ,同样条件下2mol元素硼燃烧生成1molB2O3(S),放热1264kJ。求25℃时B2O6(g)的标准摩尔生成焓。
第10题
在等温等压下,当反应的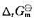 >0.5kJ·mol-1时,该反应能否进行?()
>0.5kJ·mol-1时,该反应能否进行?()
A.能正向自发进行
B.能逆向自发进行
C.不能判断
D.不能进行