 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在盐酸介质中,用KMnO4溶液滴定Fe2+时,需加入MnSO4,其主要作用是( )
A.加快反应速率
B.防止诱导效应
C.阻止MnO2生成
D.防止KMnO4分解
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.加快反应速率
B.防止诱导效应
C.阻止MnO2生成
D.防止KMnO4分解
 答案
答案
 更多“在盐酸介质中,用KMnO4溶液滴定Fe2+时,需加入MnSO4,其主要作用是() A.加快反应速率 B.防止诱导效应 C.”相关的问题
更多“在盐酸介质中,用KMnO4溶液滴定Fe2+时,需加入MnSO4,其主要作用是() A.加快反应速率 B.防止诱导效应 C.”相关的问题
第1题
第2题
含MnO2的试样0.5000g,在酸性溶液中加入0.6020g Na2C2O4,过量的Na2C2O4在酸性介质中用28.00mL c(KMnO4)=0.02000mol/L的KMnO4溶液滴定,求试样中MnO2的含量。
第4题
A.KMnO4自身是指示剂,待有足够KMnO4时才能加快滴定速度
B.O2为该反应催化剂,待有足够氧时才能加快滴定速度
C.Mn2+为该反应催化剂,待有足够Mn2+才能加快滴定速度
D.MnO2为该反应催化剂,待有足够MnO2才能加快滴定速度
第5题
称取纯As2O30.1978g,用以标定KMnO4溶液的浓度。As2O3溶解后,在酸陛介质中用KMnO4溶液滴定至计量点,消耗KMnO4溶液40.00mL。问KMnO4溶液的浓度是多少?
第6题
A.滴定过程中消耗H+,使反应速率加快
B.滴定过程中产生H+,使反应速率加快
C.滴定过程中反应物浓度越来越小,使反应速率越来越快
D.反应产生Mn2+,它是KMnO4与H2O2反应的催化剂
E.反应产生O2,使反应速率加快
第7题
甲酸钠(HCOONa)和KMnO4在中性介质中按下述反应式反应:
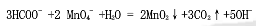 今称取HCOONa试样0.5000g,溶于水后,在中性介质中加入过量的0.06000mol·L-1KMnO4溶液50.00mL,过滤除去MnO2沉淀,以H2SO4酸化溶液后,用0.1000mol·L-1H2C2O4溶液滴定过量的KMnO4至终点,消耗25.00mL。计算试样中HCOONa的含量。[M(HCOONa)=68.00g·mol-1]
今称取HCOONa试样0.5000g,溶于水后,在中性介质中加入过量的0.06000mol·L-1KMnO4溶液50.00mL,过滤除去MnO2沉淀,以H2SO4酸化溶液后,用0.1000mol·L-1H2C2O4溶液滴定过量的KMnO4至终点,消耗25.00mL。计算试样中HCOONa的含量。[M(HCOONa)=68.00g·mol-1]
第8题
A.加K+的浓度,以加快反应速率
B.形成NaBr以防止重氮盐分解
C.使滴定终点的指示更明显
D.利用生成的Br2的颜色指示终点
E.能生成大量的NO+,从而加快反应速率
第9题