 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在994K,使纯氢气慢慢通过过量的CoO(s).则氧化物部分地被还原为Co(s).出来的平衡气体中氢的体积分数φ(H2)=0.025.在同一温度,若用co还原CoO(s),平衡后气体中一氧化碳的体积分数φ(CO)=0.0192.求等物质的量的CO和H2O(g)的混合物,在994K下通过适当催化剂进行反应,其平衡转化率为多少?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“在994K,使纯氢气慢慢通过过量的CoO(s).则氧化物部分地被还原为Co(s).出来的平衡气体中氢的体积分数φ(H2)=0.025.在同一温度,若用co还原CoO(s),平衡后气体中一氧化碳的体积分…”相关的问题
更多“在994K,使纯氢气慢慢通过过量的CoO(s).则氧化物部分地被还原为Co(s).出来的平衡气体中氢的体积分数φ(H2)=0.025.在同一温度,若用co还原CoO(s),平衡后气体中一氧化碳的体积分…”相关的问题
第1题
在994K,使纯氢气慢慢地通过过量的CoO(s),则氧化物部分地被还原为Co(s)。出来的平衡气体中氢的体积分数ψ(H2)=2.50%。在同一温度,若用CO还原CoO(s),平衡后气体中一氧化碳的体积分数ψ(CO)=1.92%。求等物质的量的一氧化碳和水蒸气的混合物在994K下,通过适当催化剂进行反应,其平衡转化率为多少?
第2题
第3题
含有20%(体积)CO和80%(体积)N2的气体混合物通过FeO层使之还原为Fe,反应式如下:

假设反应能在1000K和1bar条件下达到平衡状态,计算每分钟能生成铁的量。已知Ka=0.52,气体混合物的流量为100mol·min-1。
第4题
称取纯Fe2O3和Al2O3混合物0.5622g,在加热状态下通氢气将Fe2O3还原为Fe,此时Al2O3不改变。冷却后称量该混合物为0.4582g。计算试样中Fe、Al的质量分数。
第5题
甲烷在1bar,700℃时反应生成炭黑,计算平衡气相转化率,以及反应后纯甲烷的摩尔分数。已知温度为700℃时,Ka=7.403,反应中甲烷和氢气为气体,炭黑为固体。
第7题
一定体积的氢和氖混合气体,在27℃时压力为202kPa,加热使气体膨胀至原体积的4倍时,压力变为101kPa。问(1) 膨胀后混合气体的温度是多少?(2) 若混合气体中H2的质量分数是25.0%,原始混合气体中H2的分压是多少?(Ne原子量为20.2。)
第8题
两容器分别贮有气体A和B,温度和体积都相同,试说明在下列各种情况中它们的分子的速度分布是否相同:(1)A为氮,B为氢,而且氮和氢的质量相等,即mA=mB;(2)A和B均为氢气,但mA≠mB;(3)A和B均为氢气,而且mA=mB,但是使A的体积等温地膨胀到原体积的二倍.
第9题
A.氢气占10%
B.氢气占50%
C.氢气占29%
D.氢气占70%
第10题
CO2(g)与H2S(g)在高温的反应为CO2(g)+H2S(g)===COS(g)+H2O(g),今在610K时将4.4g的CO2(g)加入体积为2.5dm3的空瓶中,然后再充入H2S(g)使总压为1000kPa。达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析. 得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
(1)610K时的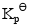 ;
;
(2)610K时的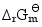 ;
;
(3)反应的标准摩尔焓变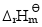 (设其不随温度而变);
(设其不随温度而变);
(4)610K时,往该体积的瓶中充入不参与反应的气体,直至压力加倍,则COS(g)的产量有何变化。若充入不参与反应的气体,保持压力不变,而使体积加倍,COS(g)的产量又有何变化。