 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知参与下面反应的各种物质298K时的标准摩尔生成热: 试计算常温下该反应的。
已知参与下面反应的各种物质298K时的标准摩尔生成热:
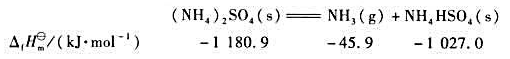
试计算常温下该反应的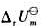 。
。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知参与下面反应的各种物质298K时的标准摩尔生成热:
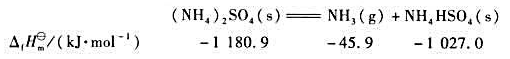
试计算常温下该反应的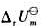 。
。
 答案
答案
 更多“已知参与下面反应的各种物质298K时的标准摩尔生成热: 试计算常温下该反应的。”相关的问题
更多“已知参与下面反应的各种物质298K时的标准摩尔生成热: 试计算常温下该反应的。”相关的问题
第1题
已知下列反应的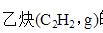 ,求298K、标准状态下AgCl的标准摩尔生成焓
,求298K、标准状态下AgCl的标准摩尔生成焓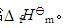 。
。
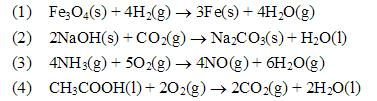
第2题
利用298K时有关物质的水合离子的标准摩尔生成焓,计算反应:Ag+(aq)+Cl—(aq)
 AgCl(s)在298K时的标准摩尔焓变。
AgCl(s)在298K时的标准摩尔焓变。
第3题
298K时,已知
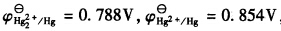 ,试计算:(1)反应Hg2++2e→
,试计算:(1)反应Hg2++2e→
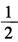 Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
第4题
已知乙烯氧化制环氧乙烷,可发生下列两个反应:
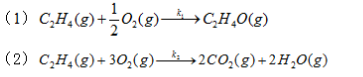
在298K时物质的标准摩尔生成Gibbs自由能数据如下:
| 物质 | C2H4O(g) | C2H4(g) | CO2(g) | H2O(g) |
| Delta _fG_m^{ominus }/(kJcdot mol^{-1}) | -13.1 | 68.1 | -394.4 | -228.6 |
当在银催化剂上,研究上述反应时得到反应(1)及反应(2)的反应级数完全相同,E1=63.6kJ·mol-1,E2=82.8kJ·mol-1,而且可以控制C2H4O(g)进一步氧化的速率极低。
第5题
已知电极反应:
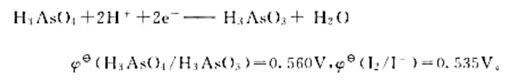
计算下列反应:
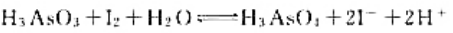
(1)在298K时的平衡常数;
(2)如果pH=7,其他物质浓度均为标准态,反应向什么方向进行?
(3)如果溶液的c(H+)=6.0mol·L-1.其他物质浓度均为标准态.反应向什么方向进行?
第6题
已知乙烯氧化制环氧乙烷,可发生下列两个反应:
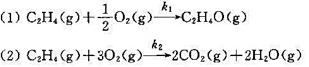
在298K时物质的标准摩尔生成Gibbs自由能数据如下:

当在银催化剂上,研究上述反应时得到反应(1)及反应(2)的反应级数完全相同,E1= ,E2=
,E2= ,而且可以控制C2H4O(g)进一步氧化的速率极低。
,而且可以控制C2H4O(g)进一步氧化的速率极低。
(1)请从热力学观点,讨论乙烯氧化生成环氧乙烷的可能性;
(2)求T1=298 K,T2= 503 K时,两反应的速率的比值r1/r2;
(3)从动力学观点,讨论乙烯氧化生成环氧乙烷是否可行,并据计算结果讨论应如何选择反应温度。
第7题
298K时,反应 的速率常数k1=4.80×104s-1,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
的速率常数k1=4.80×104s-1,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为(NzO2,g)=97.73kJ·mol-1和
(NO2,g)=51.25kJ·mol-1。请计算:
第8题
已知298K时,正辛烷C8H18(g)的标准摩尔燃烧焓为 -5512.4kJ.mol-1,二氧化碳CO2(g)和水H2O(1)的标准摩尔生成焓分别为393.5和-285.8mol-1;正辛烷C8H18(g)、氢气H2(g)和石墨C(s)的标准摩尔熵分别为463.71、130.68和5.74J.K-1.mol-1,计算 (1)298K时C8H18(g)生成反应的
1.jpg) (2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
(2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
第9题
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
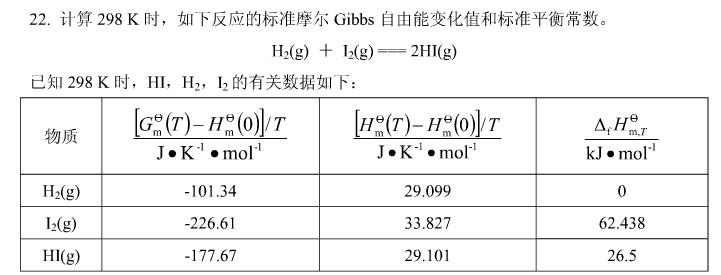
第10题
已知在298K时,下列反应:
①CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s),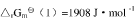
②
③C(石墨)+O2(g)===CO2(g),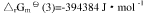
④N2(g)+3H2(g)===2NH3(g),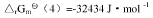 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能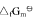 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数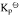 。
。