 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在800 K时,某反应的活化能为182 kJ.mol-1,加入某催化剂后,活化能降为151 kJ.mol-1,计算加入催化
剂后,该反应的速率增大了多少倍?(假定加入催化剂后指前因子不变)
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“在800 K时,某反应的活化能为182 kJ.mol-1,加入某催化剂后,活化能降为151 kJ.mol-1,计算加入催化”相关的问题
更多“在800 K时,某反应的活化能为182 kJ.mol-1,加入某催化剂后,活化能降为151 kJ.mol-1,计算加入催化”相关的问题
第1题
在800K时,某反应的活化能为182kJ·mol-1,加入某催化剂后,活化能降为151kJ·mol-1,计算加入催化剂后,该反应的速率增大了多少倍?(假定加入催化剂后指前因子不变)
第4题
反应A+B====AB的活化能是Ea,加入催化剂K后,反应历程发生变化,A+K====AK,活化能为E1,AK+B====AB+K,活化能为E2,(Ea>E2>E1)则加入催化剂后,反应的活化能为( )。
(A) E1(B) E2(C) E1+E2(D) E1-E2
第5题
在27℃时,反应H2O2→H2O+O2的活化能为75.3kJ·mol-1。若用I-催化,活化能降为56.5kJ·mol-1;若用过氧化氢酶催化,活化能降为25.1kJ·mol-1。试计算在相同温度下,该反应用I-催化和酶催化时,其反应速率分别是无催化剂时的多少倍?
第7题
第8题
乙醛分解为甲烷及一氧化碳的反应:CH3CHO→CH4+CO,500℃时活化能为190kJ·mol-1,如果用碘蒸气作催化剂,则活化能降为136kJ·mol-1,计算反应速率增加了多少倍?
第9题
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率常数。
第10题
反应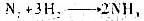 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。