 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在100ml水溶液中含有0.03mol蔗糖和0.1molHCl,用旋光计测得在301K经20分钟有32%的蔗糖发生了水解。已知其水解
为一级反应,求:
(1)反应速率常数;
(2)反应开始时和反应至20分钟时的反应速率;
(3)40分钟时已水解的蔗糖百分数。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
为一级反应,求:
(1)反应速率常数;
(2)反应开始时和反应至20分钟时的反应速率;
(3)40分钟时已水解的蔗糖百分数。
 答案
答案
 更多“在100ml水溶液中含有0.03mol蔗糖和0.1molHCl,用旋光计测得在301K经20分钟有32%的蔗糖发生了水解。已知其水解”相关的问题
更多“在100ml水溶液中含有0.03mol蔗糖和0.1molHCl,用旋光计测得在301K经20分钟有32%的蔗糖发生了水解。已知其水解”相关的问题
第1题
第2题
第3题
第4题
蔗糖催化水解是一级反应,在25℃时,若其速率常数为5.7×10-5s-1。问:
(1)浓度为1 mol.dm-3蔗糖溶液分解10%需要多少时间?
(2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
第5题
第6题
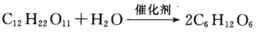 是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
是一级反应。在25℃速率常数为5.7×10-5s-1。问: (1)浓度为1mol.dm-3蔗糖溶液分解10%需要多少时间? (2)若反应活化能为110 kJ.mol-1,那么在什么温度时反应速率是25℃时的1/10。
第7题
蔗糖在稀硫酸溶液中按照下式进行水解:
C12H22O11+H2O→C6H12O6(葡萄糖)+C6H12O6(果糖)
当温度与酸的浓度一定时,反应速率与蔗糖的浓度成正比。今有一溶液,1dm3中含0.300molC12H22O11及0.1molHCl,在48℃时,20min内有x(C12H22O11)=0.32的C12H22O11水解。(1)计算反应速率系(常)数;(2)计算反应开始时(t=0)及20min时的反应速率;(3)问40min后有多少蔗糖水解?
第8题
末期反应时间与转化率
蔗糖在稀水溶液中水解生成葡萄糖和果糖的反应为
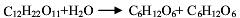

当水大大过量时,反应遵循一级反应动力学,即(-rA)=kcA,在催化剂HCl浓度为0.01mol/L,反应温度为48℃时,反应速率常数为k=0.0193min-1。当蔗糖的浓度为0.1mol/L和0.5mol/L时计算:
(1)反应20min后,上述两种初始浓度下反应液中蔗糖、葡萄糖和果糖的浓度分别为多少?
(2)试计算两种初始浓度的溶液中蔗糖的转化率各为多少?
(3)若蔗糖浓度降到0.01min/L时,两种初始浓度条件下所需反应时间各为多少?
第9题