 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某反应当温度由20℃升高至30℃时,反应速率增大了1倍,试计算该反应的活化能(kJ.mol-1)。
某反应当温度由20℃升高至30℃时,反应速率增大了1倍,试计算该反应的活化能(kJ.mol-1)。
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应当温度由20℃升高至30℃时,反应速率增大了1倍,试计算该反应的活化能(kJ.mol-1)。
 答案
答案
 更多“某反应当温度由20℃升高至30℃时,反应速率增大了1倍,试计算该反应的活化能(kJ.mol-1)。”相关的问题
更多“某反应当温度由20℃升高至30℃时,反应速率增大了1倍,试计算该反应的活化能(kJ.mol-1)。”相关的问题
第4题
A.51.2kJ·mol-1
B. 345.7kJ·mol-1
C. 22.24kJ·mol-1
D. 150.1kJ·mol-1
第5题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第6题
已知某平行反应
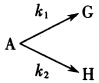 的活化能和指前因子如下,问:(1)温度升高时,哪个反应的速率常数增加得更快(指倍率)?(2)温度升高能否使k1>k2?(3)当温度从300K上升至1000K时,产物G与H之比值将增大还是减小?改变多少倍?
的活化能和指前因子如下,问:(1)温度升高时,哪个反应的速率常数增加得更快(指倍率)?(2)温度升高能否使k1>k2?(3)当温度从300K上升至1000K时,产物G与H之比值将增大还是减小?改变多少倍?

第7题
若某反应的活化能为80kJ·mol-1,则反应温度由20℃增加到30℃,其反应速率常数约为原来的
(A) 2倍 (B) 3倍 (C) 4倍 (D) 5倍
第8题
第10题
温度为500K时,某理想气体恒容反应的速率常数 则此反应用压力表示的反应速率常数kp=().
则此反应用压力表示的反应速率常数kp=().