 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
将一块纯铜片置于0.050mol•L-1AgNO3溶液中。计算溶液达到平衡后的组成。(提示:首先计算出反应平衡常数。)
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“将一块纯铜片置于0.050mol•L-1AgNO3溶液中。计算溶液达到平衡后的组成。(提示:首先计算出反应平衡常数。)”相关的问题
更多“将一块纯铜片置于0.050mol•L-1AgNO3溶液中。计算溶液达到平衡后的组成。(提示:首先计算出反应平衡常数。)”相关的问题
第1题
将一块纯铜片置于0.050mol·L-1AgNO3溶液中。计算溶液达到XF衡后的组成。
(提示:首先计算出反应平衡常数。)
第2题
将一块纯铜片置于0.050mol/L AgNO3溶液中,计算溶液达到平衡后的组成。已知 (Cu2+/Cu)=0.337V,
(Cu2+/Cu)=0.337V, (Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)
(Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)
第3题
第4题
将固体AgBr和AgCl加入50.0mL纯水中,不断搅拌使其达到平衡。计算溶液中Ag+的浓度。
第5题
将固体AgBr和AgCl加入到50.0mL纯水中,不断搅拌使其达到平衡。计算溶液中Ag+的浓度。
第6题
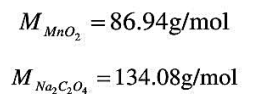 。
。
第7题
 其他数据查附表.
其他数据查附表.(1)计算 ;
;
(2)将Cl2(g)通入[Fe(bipy)3]2+溶液中,Cl2能否将其氧化?写出反应方程式,并计算25℃下该反应的标准平衡常数Kθ;
(3)若溶液中[Fe(bipy)3]2+的依度为0.20mol·L-1,所通Cl2的压力始终保持100.0KθPa,求平衡时溶液中各离子浓度.
第8题
称取软锰矿0.3216g和分析纯的Na2C2O40.3685g,共置于同一烧杯中,加入H2SO4,并加热;待反应完全后,用0.02400mol/L KMnO4溶液滴定剩余的Na2C2O4,消耗KMnO4溶液11.26mL。计算软锰矿中MnO2的质量分数。
第9题